

![]()
Criptococosis
 La
criptococosis, habitualmente producida por Cryptococcus neoformans var neoformans,
es la cuarta enfermedad infecciosa grave, en orden de frecuencia en los Estados
Unidos y Europa. Sólo superada por la neumocistosis, las infecciones
por Citomegalovirus y por Mycobacterium avium-intracelullare. En los países
en desarrollo la incidencia de la criptococosis es mayor. En Africa Central
es, junto con la tuberculosis, la infección más común.
Se calcula que entre el 3 y el 5 % de los enfermos con SIDA padecen criptococosis
en Europa. Esta proporción se eleva del 6 al 10 % en los Estados Unidos
y Brasil y alrededor del 20 % en Africa Central. En Argentina, si bien no existen
cifras oficiales, la frecuencia de la criptococosis en enfermos HIV positivos,
rondaría el 15 %. Sólo el Hospital F. J. Muñiz recibe más
de 130 casos nuevos por año (8).
La
criptococosis, habitualmente producida por Cryptococcus neoformans var neoformans,
es la cuarta enfermedad infecciosa grave, en orden de frecuencia en los Estados
Unidos y Europa. Sólo superada por la neumocistosis, las infecciones
por Citomegalovirus y por Mycobacterium avium-intracelullare. En los países
en desarrollo la incidencia de la criptococosis es mayor. En Africa Central
es, junto con la tuberculosis, la infección más común.
Se calcula que entre el 3 y el 5 % de los enfermos con SIDA padecen criptococosis
en Europa. Esta proporción se eleva del 6 al 10 % en los Estados Unidos
y Brasil y alrededor del 20 % en Africa Central. En Argentina, si bien no existen
cifras oficiales, la frecuencia de la criptococosis en enfermos HIV positivos,
rondaría el 15 %. Sólo el Hospital F. J. Muñiz recibe más
de 130 casos nuevos por año (8).
Desde el advenimiento de la pandemia del SIDA, la epidemiología de la criptococosis sufrió varias modificaciones. Su incidencia se incrementó de 40 a 50 veces. En el Hospital Muñiz se diagnosticaban, en promedio, 2 ó 3 casos por año hasta 1985; se elevó a 80 hasta 1991 y con posterioridad la incidencia no fue menor a 120 casos por año. La edad promedio descendió, de más de 40 años en los pacientes HIV negativos, a 28.3 años en los HIV positivos. La relación hombre/mujer es similar a la del SIDA. Comenzó siendo superior a 12:1 y actualmente es 4:1. Entre las conductas favorecedoras de la infección por el HIV en la República Argentina, destacan: la elevada frecuencia de adictos a drogas por vía venosa, 71 % de los casos, las relaciones homo y bisexuales y la transmisión heterosexual y por hemoderivados. La gran mayoría de los casos de criptococosis asociadas al SIDA, en Buenos Aires, han sido producidas por C. neoformans var neoformans, de serotipo A (3, 8, 45). La otra variedad de esta especie, C. neoformans var gatti, de serotipos B y C, ha sido señalada en la Argentina como agente causal del 20 % de la criptococosis en pacientes HIV negativos, y excepcionalmente se la ha visto asociada al SIDA. La variedad gatti predomina en zonas tropicales del mundo, y ha sido encontrada con elevada frecuencia en el sur de California, donde se producía el 43 % de los casos antes de 1983, en Brasil, Africa ecuatorial y Australia. Aún en estas zonas la mayor parte de los casos asociados al SIDA son producidos por el serotipo A de la variedad neoformans, en tanto que los ocasionados por C. neoformans var gatti son minoría (36, 59). Catorce de los 27 casos de criptococosis producida por C. neoformans var gatti asociadas al SIDA, han sido diagnosticados en países en desarrollo, especialmente Brasil, donde el serotipo predominante es el B (40).
La terapéutica antirretroviral actual ha disminuido la incidencia criptococosis en los países industrializados, donde la frecuencia de esta complicación del SIDA ya era baja. Por el contrario, su impacto ha sido mínimo en los países en desarrollo, con una alta incidencia de esta micosis (24, 40).
La elevada frecuencia de
criptococosis como enfermedad asociada al SIDA hace suponer que la infección
asintomática por C. neoformans debe ser más común de lo
que se sospechaba. La mayor incidencia de casos en países en vías
de desarrollo se correlaciona con una mayor exposición a fuentes de infección.
Esto último ha sido explicado por la abundancia de excrementos de palomas
y otras aves en lugares sombríos y reparados, maderas contaminadas, calles
sin asfaltar y la posibilidad de la dispersión de blastoconidias o basidiosporos
por el aire (59, 66, 69).
El SIDA predispone más
que otras enfermedades, que producen déficit de la inmunidad mediada
por células, a la criptococosis diseminada. Los componentes de la cápsula
del C. neoformans: glucoróxidomananos, galactóxidomananos y mananoproteínas,
son los responsables de su virulencia, al alterar los mecanismos de la fagocitosis.
La saturación de antígeno capsular, común en los pacientes
HIV positivos, determina la formación de inmunocomplejos e impide la
libre acción de los anticuerpos específicos. Por el contrario,
se detectan tasas de antigenemia y antigenorraquia 100 veces más elevadas
que las observadas en los pacientes seronegativos (9, 34, 36, 66).
El exceso de antígeno
capsular bloquea la acción de los linfocitos T "helper", CD4
positivos, así como la de los macrófagos efectores; ocasiona la
activación de las células supresoras, CD8 positivas e incrementa
la actividad policlonal de los linfocitos B, con una reacción anárquica
del sistema inmune humoral. Estas acciones sobre la inmunidad son similares
a las producidas por el HIV, ambos actuarían sinérgicamente, deteriorando
el estado inmunitario del paciente y reduciendo sus posibilidades de supervivencia
(59, 66).
Respecto a las manifestaciones
clínicas, cabe destacar que la criptococosis asociada al SIDA es una
infección sistémica, con ataque multiorgánico, evolución
aguda o subaguda, elevada frecuencia de compromiso meningoencefálico,
pronóstico muy grave por su escasa respuesta a los antifúngicos
y alta tasa de recaídas (8).
La experiencia de 114 pacientes
observados en el Hospital F. J. Muñiz hasta el año 1992, indica
que el cuadro infeccioso general fue comprobado en 96.5 % de los pacientes,
con el siguiente orden decreciente de signos y síntomas: fiebre, astenia,
pérdida de peso, anemia, hepatosplenomegalia y adenomegalias. Un 10 %
de los casos sólo tienen estas manifestaciones poco características,
y que pueden ser confundidas con las ocasionadas por el HIV. El síndrome
neurológico se presenta en el 90.4 % de casos; la mayor parte de las
veces sólo refieren cefalea persistente, vómitos, fotofobia y
un síndrome meningeo incompleto. Las alteraciones de la conciencia y
las convulsiones son signos de mal pronóstico. Las manifestaciones de
foco, tales como parálisis del recto externo, afasia, síndrome
cerebeloso, paresias de los miembros, etc, aparecen con poca frecuencia (8).
 La
persistencia de fiebre y cefalea durante 1 semana, debe ser motivo suficiente
de sospecha e indica la necesidad de realizar una punción raquídea.
El LCR fluye, en goteo rápido o en chorro, debe tomarse sistemáticamente
la presión de apertura, el líquido es cristal de roca y suele
presentar muy escasas alteraciones físico-químicas y citológicas.
Los recuentos de leucocitos, habitualmente, son inferiores a 20/µl, las
proteínas están ligeramente elevadas y la glucorraquia generalmente
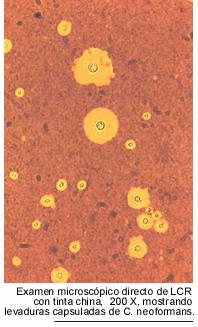
es normal. Por el contrario, el examen microscópico directo, del sedimento
de LCR, con tinta china, acusa la presencia de levaduras capsuladas en el 80
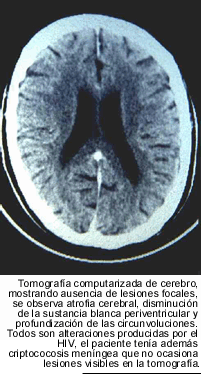
% de las muestras. La tomografía computarizada del encéfalo no
exhibe, habitualmente, masas ocupantes. Las alteraciones observadas suelen ser
las determinadas por el HIV: atrofia cerebral, aumento del espacio subaracnoideo,
así como del tamaño de los ventrículos y con menos frecuencia,
signos de vasculitis. La resonancia nuclear magnética, muestra en algunos
casos la presencia de pequeñas lesiones nodulares situadas en la base
del encéfalo.
La
persistencia de fiebre y cefalea durante 1 semana, debe ser motivo suficiente
de sospecha e indica la necesidad de realizar una punción raquídea.
El LCR fluye, en goteo rápido o en chorro, debe tomarse sistemáticamente
la presión de apertura, el líquido es cristal de roca y suele
presentar muy escasas alteraciones físico-químicas y citológicas.
Los recuentos de leucocitos, habitualmente, son inferiores a 20/µl, las
proteínas están ligeramente elevadas y la glucorraquia generalmente
es normal. Por el contrario, el examen microscópico directo, del sedimento
de LCR, con tinta china, acusa la presencia de levaduras capsuladas en el 80
% de las muestras. La tomografía computarizada del encéfalo no
exhibe, habitualmente, masas ocupantes. Las alteraciones observadas suelen ser
las determinadas por el HIV: atrofia cerebral, aumento del espacio subaracnoideo,
así como del tamaño de los ventrículos y con menos frecuencia,
signos de vasculitis. La resonancia nuclear magnética, muestra en algunos
casos la presencia de pequeñas lesiones nodulares situadas en la base
del encéfalo.
El examen de fondo de ojos
debe realizarse sistemáticamente y puede mostrar edema de papila, borramiento
de sus bordes o signos de coriorretinitis; en los casos más graves suele
haber atrofia del nervio óptico. En pacientes con hipertensión
endocraneana grave, puede producirse la pérdida brusca de la agudeza
visual. Sin embargo, este hecho es más común en las infecciones
debidas a C. neoformans var. gattii.
La sintomatología
respiratoria estuvo presente en el 44.7 % de 114 pacientes estudiados en el
Hospital Muñiz. Estas manifestaciones son poco específicas, y
a veces son ocasionadas por otras infecciones concomitantes, como neumocitosis
y tuberculosis. Clínicamente produce tos, expectoración mucosa
o mucopurulenta, disnea, dolor torácico y raras veces hemoptisis. Radiológicamente
se observan infiltrados pulmonares difusos y bilaterales, infiltrados intersticiales
micronodulillares de tipo miliar, imágenes nodulares solitarias, cavidades
y derrames pleurales. Estos últimos se observaron en dos de 22 casos
de criptococosis respiratoria, examinados recientemente y el derrame pleural
era serofibrinoso (30).
El diagnóstico de
criptococosis pulmonar presenta dificultades, ya que el hallazgo de C. neoformans
en el esputo o las secreciones broncoaspiradas no son pruebas suficientes para
asegurar que se trata de una criptococosis pulmonar. Este último diagnóstico
sólo puede certificarse por la biopsia pulmonar. Sin embargo, al analizar
los datos de 22 pacientes, hemos podido concluir que en el caso de los enfermos
con SIDA, con recuentos de linfocitos CD4 inferiores a 200/µL, la presencia
de C. neoformans en las secreciones respiratorias obliga a realizar hemocultivos
por lisis-centrifugación, estudio de LCR y determinación de antigenemia,
a fin de diagnosticar una criptococosis diseminada que haya pasado inadvertida
(30).
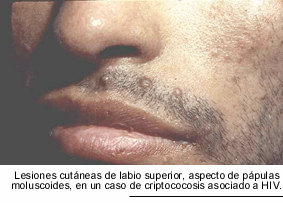
El 6 % de los enfermos presentan
lesiones cutáneas, éstas son únicas o múltiples,
papulosas y de aspecto moluscoide. En oportunidades se ha comprobado, en la
misma lesión, la presencia de C. neoformans y Molluscum contagiosum,
así como de C. neoformans e H. capsulatum. Con menor frecuencia se comprueban
úlceras que asientan sobre una placa infiltrada.
 Las
linfadenopatías diseminadas son también observadas en la criptococosis
asociada al SIDA, no tienen nada de típico y sólo el hallazgo
de Cryptococcus en la punción-aspiración de los ganglios o en
las biopsias, permite el diagnóstico. Otras localizaciones son hepatitis,
pericarditis, miocarditis y prostatitis. Esta última tiene gran importancia
porque se estima que la próstata es un reservorio de Cryptococcus, aún
después del tratamiento exitoso y que puede ser el punto de partida de
las frecuentes recaídas de esta afección (36, 59). No es común
la observación de lesiones óseas en la criptococosis asociada
al SIDA, sin embargo, la médula ósea es habitualmente invadida
por C. neoformans (3).
Las
linfadenopatías diseminadas son también observadas en la criptococosis
asociada al SIDA, no tienen nada de típico y sólo el hallazgo
de Cryptococcus en la punción-aspiración de los ganglios o en
las biopsias, permite el diagnóstico. Otras localizaciones son hepatitis,
pericarditis, miocarditis y prostatitis. Esta última tiene gran importancia
porque se estima que la próstata es un reservorio de Cryptococcus, aún
después del tratamiento exitoso y que puede ser el punto de partida de
las frecuentes recaídas de esta afección (36, 59). No es común
la observación de lesiones óseas en la criptococosis asociada
al SIDA, sin embargo, la médula ósea es habitualmente invadida
por C. neoformans (3).
La mayor parte de los pacientes con criptococosis presenta una enfermedad por HIV muy avanzada, los recuentos de células CD4 son inferiores a 200/µl, sin embargo, la criptococosis es la primer enfermedad marcadora en la mitad de los enfermos. La lista de infecciones concomitantes es larga, se destacan por su elevada frecuencia la tuberculosis, la neumocistosis, las diarreas y las infecciones por virus de la familia Herpetoviridae.
Referente al diagnóstico,
sobresale la importancia del examen microscópico directo del sedimento
del LCR con tinta china, positivo en más del 80 % de los casos y los
cultivos que son positivos en el 90 % de los pacientes. Los hemocultivos, realizados
por la técnica de lisis-centrifugación con saponina, permiten
el diagnóstico del 67 % de los pacientes y los resultados pueden obtenerse
en menos de una semana. Los urocultivos, así como el examen microscópico
del sedimento urinario, facilitan la demostración del C. neoformans en
el 30 a 40 % de los enfermos. Su eficacia es mayor después del masaje
prostático (3, 10, 43).
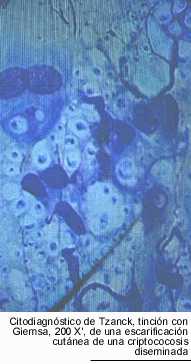
Otros materiales útiles
pueden ser biopsias de médula ósea o hepática, punción-aspiración
de ganglios linfáticos, mielocultivos, escarificaciones o biopsias cutáneas,
etc.(3).
La demostración del antígeno capsular del C. neoformans en los
fluidos orgánicos es un instrumento de diagnóstico de gran importancia.
Se lleva a cabo por dos técnicas: la aglutinación de partículas
de latex sensibilizadas con gamma-globulina de conejo anti-polisacárido
capsular o por la prueba de ELISA. Los estudios comparativos de ambas reacciones
han demostrado que sus resultados coinciden en la mayoría de los casos.
La prueba de aglutinación es más simple en su realización
y más económica (3, 8, 12).
La antigenemia es positiva
en más del 95 % de los pacientes, la antigenorraquia acusa la presencia
de polisacáridos capsular en el 93 % de los enfermos (su sensibilidad
es equivalente a la de los cultivos del LCR) y el 82 % de los pacientes exhiben
antigenuria positiva. Con los equipos actuales, la especificidad de esta reacción
es muy alta y llega a ser absoluta en el LCR (3, 12).
Actualmente, se considera que el tratamiento de elección para la criptococosis asociada al SIDA, es la asociación de anfotericina Bpor vía intravenosa, a razón de 0.7 a 0.8 mg/kg/día y 5-fluorocitosina por vía oral o intravenosa, a razón de 100 mg/kg/día, durante 2 semanas. Con este esquema inicial más del 80 % de los pacientes esteriliza el LCR, aún si esta meta no se obtuvo, es muy difícil que después de este plazo, el paciente presenta manifestaciones graves de criptococosis. Por lo tanto, después de la segunda semana, se le indica fluconazol por vía oral, a razón de 400 mg/día, por un lapso de diez semanas (42, 50). En un estudio se comparó la eficacia del fluconazol y el itraconazol en esta fase del tratamiento, si bien los resultados fueron bastante similares, el fluconazol obtuvo mayor número de pacientes con LCR estéril (55). Se recomienda controlar siempre la presión de apertura del LCR y cuando ésta excede los 250 mm de agua, debe indicarse la realización de punciones lumbares evacuatorias repetidas en forma diaria o día por medio, con la extracción de 20 a 25 mL de LCR. También puede efectuarse, en estos casos, el drenaje quirúrgico a nivel lumbar o de los ventrículos cerebrales. Este esquema terapéutico ha reducido la mortalidad de la criptococosis asociada al SIDA, desde un 20 a 30 % en la década pasada, a un 6 a 15 % en la actualidad (67).
Sin embargo, este esquema
terapéutico no puede ser indicado en un buen número de países
en los que no se comercializa la 5-fluorocitosina. Se recurre entonces a la
segunda elección, a la administración de anfotericina B por vía
intravenosa, en la dosis de 0.8 mg/kg/día, durante 6 a 8 semanas. Esta
alternativa es menos eficaz que la anterior y tiene mayores efectos colaterales,
en especial, trombosis venosas, anemia grave y toxicidad renal.
Otra posibilidad es indicar
el fluconazol por vía oral o intravenosa, las dosis diarias varían
de 400 a 800 mg, y deben mantenerse por 10 a 12 semanas. Esta droga es muy bien
tolerada pero, administrada como tratamiento inicial y a la dosis de 400 mg/día,
sólo produce la remisión clínica completa en el 20 % de
los pacientes. Sin embargo, su eficacia aumenta cuando se emplean dosis más
elevadas, actualmente se aconseja indicar 1.600 mg por vía intravenosa
el primer día de tratamiento, seguido de la administración de
800 mg diarios por vía oral ó itravenosa durante 12 semanas. Con
este esquema se consigue la esterilización del LCR en un lapso medio
de 21 días y en el 83 % de los casos tratados (12, 50).
También se ha estudiado
la eficacia de la administración conjunta del fluconazol en dosis de
400 mg/día con la 5-fluorocitosina a razón de 150 mg/kg/día,
durante 10 semanas. Este esquema consiguió remisiones clínicas
y micológicas en el 63 % de los casos, y se obtuvo la esterilización
del LCR en un lapso medio de 23 días (42).
Con el objeto de reducir
la toxicidad de la anfotericina B, se ha utilizado la administración
de esta droga antifúngica asociada a Intralipid, liposomas y complejos
lipídicos. La anfotericina B asociada a Intralipid, reduce la toxicidad
renal del fármaco, pero no aumenta su eficacia (32). La anfotericina
B liposomal resultó ser superior a la anfotericina B desoxicolato al
producir la esterilización del LCR en un plazo de sólo dos semanas
y tener una eficacia clínica ligeramente mayor. Por el contrario, la
anfotericina B con complejos lipídicos, resultó ser menos eficaz,
probablemente debido al hecho de que estos complejos lipídicos de gran
tamaño no atraviesan la barrera hemato-encefálica (50).
 La
mayor parte de los fallecimientos por criptococosis meníngea se producen
en las primeras tres semanas posteriores al diagnóstico. Pese al tratamiento,
puede producirse la muerte de un número significativo de enfermos con
cuadros de hipertensión endocraneana grave. La administración
de anfotericina B durante estas primeras semanas, en cualquiera de los esquemas
antes señalados, disminuye el número de decesos. Como ya se señaló,
el control de hipertensión endocraneana es fundamental para la supervivencia
del enfermo y las medidas adecuadas son aquellas que permiten evacuar el LCR,
la administración de corticosteroides en altas dosis o acetazolamina
no proporcionan resultados satisfactorios (67).
La
mayor parte de los fallecimientos por criptococosis meníngea se producen
en las primeras tres semanas posteriores al diagnóstico. Pese al tratamiento,
puede producirse la muerte de un número significativo de enfermos con
cuadros de hipertensión endocraneana grave. La administración
de anfotericina B durante estas primeras semanas, en cualquiera de los esquemas
antes señalados, disminuye el número de decesos. Como ya se señaló,
el control de hipertensión endocraneana es fundamental para la supervivencia
del enfermo y las medidas adecuadas son aquellas que permiten evacuar el LCR,
la administración de corticosteroides en altas dosis o acetazolamina
no proporcionan resultados satisfactorios (67).
El itraconazol es un compuesto
triazólico, altamente eficaz frente al C. neoformans, pero con mal pasaje
a través de la barrera hemato-encefálica. Sus resultados en la
criptococosis asociada al SIDA, han sido dispares y, en general, son considerados
inferiores a los obtenidos con el fluconazol. Debe recordarse que el itraconazol
presenta interacción con varias drogas de metabolización hepática
elevada como la rifampicina y algunas drogas antirretrovirales inhibidoras de
las proteasas. Esto impide su empleo más generalizado (42, 50).
El valor de los anticuerpos específicos en el tratamiento de la criptococosis, ha sido demostrado en modelos experimentales en animales. En la actualidad, se están preparando anticuerpos monoclonales humanizados, contra la cápsula de C. neoformans para ser empleados en la terapéutica clínica. Estos anticuerpos producen descenso de la hipertensión endocraneana y de los niveles de polisacárido capsular en los fluidos orgánicos (12).
La supervivencia de los
enfermos con criptococosis asociada al SIDA es corta, a pesar del tratamiento.
En nuestro medio continúa observándose una tasa de letalidad del
35 % durante las primeras 3 ó 4 semanas, y la mayor parte de los restantes
enfermos, sólo sobreviven 12 a 18 meses.
Se consideran signos de
mal pronóstico, la presión de apertura elevada del LCR, las antigenemias
y antigenorraquias superiores a 1/1.000, los cultivos de C. neoformans en varios
materiales (LCR, sangre, esputo, punción aspiración de ganglio,
etc), la presencia de menos de 8 células/µl en el sedimento del
LCR, la alteración del estado de conciencia, los signos de hipertensión
endocraneana, los recuentos de linfocitos CD4 inferiores a 50/µL y de
linfocitos CD8 menores a 150/µL (9, 12, 42). Se estudiaron las citoquinas
en sangre y LCR de pacientes con criptococosis asociada al SIDA, a fin de ver
si algunas de estas sustancias eran indicadoras de mal pronóstico. Pudo
concluirse que los dosajes de TNF-µ por encima de los 50 pg/ml eran un
indicador de mala evolución clínica. También se encontraron
bajos niveles de IL-1 en la mayor parte de estos enfermos que tuvieron una rápida
evolución fatal (5).
 El
parámetro más eficaz para controlar la evolución de la
criptococosis con el tratamiento, es la negativización de los cultivos
del LCR. La antigenemia y la antigenorraquia descienden muy lentamente, y sólo
se tornan negativas después de muchos meses. Las recaídas post-terapéuticas
son muy frecuentes, y se presentan en alrededor del 80 % de los enfermos. Por
esta razón, es indispensable indicar un tratamiento supresivo o profilaxis
secundaria. Habitualmente, se utilizan 200 mg diarios de fluconazol, durante
lapsos superiores a un año. Este tratamiento demostró ser superior
a la administración semanal de anfotericina B en dosis de 50 mg y al
itraconazol por vía oral en dosis de 400 mg diarios (16).
El
parámetro más eficaz para controlar la evolución de la
criptococosis con el tratamiento, es la negativización de los cultivos
del LCR. La antigenemia y la antigenorraquia descienden muy lentamente, y sólo
se tornan negativas después de muchos meses. Las recaídas post-terapéuticas
son muy frecuentes, y se presentan en alrededor del 80 % de los enfermos. Por
esta razón, es indispensable indicar un tratamiento supresivo o profilaxis
secundaria. Habitualmente, se utilizan 200 mg diarios de fluconazol, durante
lapsos superiores a un año. Este tratamiento demostró ser superior
a la administración semanal de anfotericina B en dosis de 50 mg y al
itraconazol por vía oral en dosis de 400 mg diarios (16).
Si bien, la Organización
Panamericana de la Salud considera que no hay suficientes evidencias para aconsejar
la supresión de la profilaxis secundaria con fluconazol en la criptococosis,
hay numerosos datos a favor de esta posibilidad. Cuando se administra el tratamiento
antirretroviral de alta eficacia y se consigue tornar indetectable la carga
viral durante 6 meses, con restauración de la respuesta inmune, demostrada
por recuentos de linfocitos T CD4 de 200/µL, las posibilidades de recaídas
son casi nulas (16, 24, 48).
En relación a la profilaxis primaria, ésta ha sido estudiada en enfermos con recuentos de linfocitos CD4 iguales o inferiores a 100/µL. Pudo comprobarse que la administración preventiva de fluconazol en dosis de 200 mg/día, redujo la frecuencia de criptococosis meníngea y candidiasis esofágica. Otro estudio similar demostró la eficacia de este esquema profiláctico, en pacientes con recuentos del linfocitos CD4 inferiores a 68/µL. Pese a estas observaciones, la profilaxis primaria no se indica habitualmente en los pacientes con SIDA, debido a la relativa baja frecuencia de esta enfermedad, a la posibilidad de aumentar la resistencia microbiana de Candida y Cryptococcus al fluconazol, a las interacciones con otras drogas habitualmente indicadas en estos casos y al alto costo del tratamiento. Estas consideraciones no son enteramente válidas para países como la República Argentina, donde la incidencia de criptococosis es elevada y hay una gran proporción de personas HIV positivas que no siguen el tratamiento antirretroviral de alta eficacia (48, 49).
![]()